Joseph Louis Proust adalah seorang ahli kimia Prancis. Ia mendalami analisis kimia dan menjadi terkenal setelah menemukan "Hukum Perbandingan Tetap" untuk senyawa. Sebagai ilustrasi, Pada percobaan 1, 0.21 gram Besi dan 0.12 gram Belerang bereaksi membentuk 0.33 gram Besi Sulfida. 0.33 merupakan penjumlahan dari 0.21 dan 0.12. Artinya, semua reaktan berubah menjadi produk.
Pada percoban 2, 0.32 gram Besi dan 0.16 gram Belerang bereaksi membentuk 0.44 gram Besi Sulfida dan 0.04 gram Besi. Bukan 0.48 gram Besi Sulfida. Artinya, tidak semua reaktan berubah menjadi produk, ada sisa reaktan, yaitu Besi. Jika massa Besi berkurang sebesar 0.04 gram maka 0.28 gram Besi dan 0.16 gram Belerang akan membentuk 0.44 gram Besi Sulfida
Pada percobaan 3. 0.35 gram Besi dan 0.25 gram Belerang bereaksi membentuk 0.55 gram Besi Sulfida dan 0.05 gram Belerang, bukan 0.6 gram Besi Sulfida. Artinya, tidak semua reaktan berubah menjadi produk. Ada sisa reaktan, yaitu Belerang. Jika massa Belerang berkurang sebesar 0.05 gram maka 0.35 gram Besi dan 0.2 gram Belerang akan membentuk 0.55 gram Besi Sulfida
Selanjutnya tempatkan data tersebut pada tabel. Kolom 1 adalah massa Besi, tabel 2 adalah massa Belerang, dan tabel 3 adalah massa Besi Sulfida. Bagi semua nilai pada baris 1 (0.21:0.12:0.33) dengan 0.03. Proses ini akan menghasilkan nilai 7:4:11. Bagi semua nilai pada baris 2 (0.28:0.16:0.44) dengan 0.04. Proses ini akan menghasilkan nilai 7:4:11. Bagi semua nilai pada baris 3 (0.35:0.20:0.55) dengan 0.05.Proses juga menghasilkan nilai yang sama, yaitu: 7:4:11. Dari sini Kita bisa menyimpulkan bahwa perbandingan massa Besi dan Belerang untuk menghasilkan Besi Sulfida adalah sama, yaitu: 7:4:11. Inilah yang dimaksud sebagai Hukum Perbandingan Tetap.
Pada seri ini, Kita akan belajar untuk memahami apa sih Hukum Perbandingan Tetap itu dengan menyelesaikan beberapa soal. Untuk melihat jawaban dari soal ini, klik tombol "lihat jawaban". Kamu akan diarahkan menuju kanal youtube "Catatan Si Rebiaz". Video ini sangat ringan, berdurasi sekitar 3 menit, ukuran filenya juga sangat kecil, nyaman untuk ditonton bagi semua kalangan. Jika kamu memiliki soal yang berbeda, Kamu bisa menuliskannya pada kolom komentar. Mungkin saja soal kamu akan dibahas pada tutorial selanjutnya.
Pada percoban 2, 0.32 gram Besi dan 0.16 gram Belerang bereaksi membentuk 0.44 gram Besi Sulfida dan 0.04 gram Besi. Bukan 0.48 gram Besi Sulfida. Artinya, tidak semua reaktan berubah menjadi produk, ada sisa reaktan, yaitu Besi. Jika massa Besi berkurang sebesar 0.04 gram maka 0.28 gram Besi dan 0.16 gram Belerang akan membentuk 0.44 gram Besi Sulfida
Pada percobaan 3. 0.35 gram Besi dan 0.25 gram Belerang bereaksi membentuk 0.55 gram Besi Sulfida dan 0.05 gram Belerang, bukan 0.6 gram Besi Sulfida. Artinya, tidak semua reaktan berubah menjadi produk. Ada sisa reaktan, yaitu Belerang. Jika massa Belerang berkurang sebesar 0.05 gram maka 0.35 gram Besi dan 0.2 gram Belerang akan membentuk 0.55 gram Besi Sulfida
Selanjutnya tempatkan data tersebut pada tabel. Kolom 1 adalah massa Besi, tabel 2 adalah massa Belerang, dan tabel 3 adalah massa Besi Sulfida. Bagi semua nilai pada baris 1 (0.21:0.12:0.33) dengan 0.03. Proses ini akan menghasilkan nilai 7:4:11. Bagi semua nilai pada baris 2 (0.28:0.16:0.44) dengan 0.04. Proses ini akan menghasilkan nilai 7:4:11. Bagi semua nilai pada baris 3 (0.35:0.20:0.55) dengan 0.05.Proses juga menghasilkan nilai yang sama, yaitu: 7:4:11. Dari sini Kita bisa menyimpulkan bahwa perbandingan massa Besi dan Belerang untuk menghasilkan Besi Sulfida adalah sama, yaitu: 7:4:11. Inilah yang dimaksud sebagai Hukum Perbandingan Tetap.
Pada seri ini, Kita akan belajar untuk memahami apa sih Hukum Perbandingan Tetap itu dengan menyelesaikan beberapa soal. Untuk melihat jawaban dari soal ini, klik tombol "lihat jawaban". Kamu akan diarahkan menuju kanal youtube "Catatan Si Rebiaz". Video ini sangat ringan, berdurasi sekitar 3 menit, ukuran filenya juga sangat kecil, nyaman untuk ditonton bagi semua kalangan. Jika kamu memiliki soal yang berbeda, Kamu bisa menuliskannya pada kolom komentar. Mungkin saja soal kamu akan dibahas pada tutorial selanjutnya.
SOAL HUKUM PERBANDINGAN TETAP
- Jika direaksikan 2.4 gram zat A dengan 7.2 gram zat B. Sehingga, terbentuk 5.76 gram senyawa AB. Berapakah perbandingan massa A dan B pada senyawa tersebut?
- A. 2 banding 3
- B. 3 banding 4
- C. 3 banding 5
- D. 5 banding 6
- E. 5 banding 8
- Perbandingan massa Magnesium dan Oksigen dalam MgO adalah 3:2. Jika 21 gram Magnesium bereaksi kimia dengan 12 gram Oksigen. Maka reaktan yang tersisa adalah?
- A. Magnesium
- B. Oksigen
- C. Tiak ada sisa reaktan
- D. Tidak bisa ditentukan
- E. Tidak bereaksi kimia
- Perbandingan massa Besi terhadap Belerang dalam senyawa FeS adalah 7 banding 4. Berapakah sisa reaktan, jika 32 gram Besi Bereaksi dengan 16 gr Belerang?
- A. 4 gr Besi
- B. 4 gr Belerang
- C. 5 gr Besi
- D. 5 gr Belerang
- E. 6 gr Besi
- Tabel berikut menunjukkan hasil eksperiment reaksi pembentukan Magnesium Oksida. Pertanyaannya adalah berapakah massa x pada tabel tersebut?
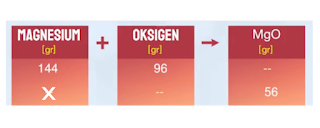
- A. 11.2 gram
- B. 22.4 gram
- C. 33.6 gram
- D. 44.8 gram
- E. 56.0 gram
Pemateri: Rebiaz
Jawaban: Hukumn Perbandingan Tetap
Sumber: https://www.youtube.com/@CatatanSiRebiaz
Komentar
Posting Komentar